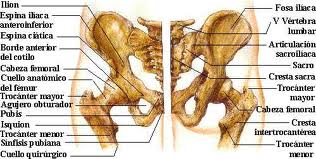
La articulación de la cadera es una diartrósis que funciona rotando la cabeza femoral, de forma prácticamente esférica, dentro de una cavidad cóncava, el acetábulo, llegando a crear un ángulo de hasta 130º mas o menos.
Ambos huesos están recubiertos de un tejido cartilaginoso formado por condrocitos que confieren el llamado cartílago articular. Dicho cartílago le da la elasticidad y resistencia mecánica a la articulación, pero en caso de lesión, tiene muy mala regeneración, ya que este cartílago no tiene vascularización y las células de las que está formado, a partir de la edad adulta, no se regeneran.
La mayor parte de las patologías que requieren intervención quirúrgica en la cadera son por alteraciones en la
articulación, bien por traumatismo, bien por problemas degenerativos.
Gluck en 1890 realiza una artroplastia total de la cadaera, utilizando marfil como sustituto articular.
En 1923, Smith Petersen cubrió la cabeza femoral remodelada con una copa de vidrio, sustituyendola posteriormente por su fragilidad por baquelita.en 1940, Moore y Bohlman emplean una prótesis cervicocefálica de acero inoxidable para el tratamiento de un paciente con un tumor del extremo proximal del fémur.
Los hermanos Judet informan de los resultados obtenidos en 300 pacientes tratados con una prótesis realizada en polimetacrilato; posteriomente utilizaron también el nailon y el vitalio para la fabricación de las prótesis.
En 1950, Thompson crea la prótesis parcial que todavía se utiliza en la actualidad.Pero fue, en 1952, el profesor John Charney quien inicia el desarrollo de os sistemas protésicos cementados, utilizando un tallo femoral de acero inoxidable con una cabeza de 22 mm de diámetro, todo en una pieza; el componente cotiloideo era de teflón, fijando ambor componentes concemento. Suguiéndole, Müller creó en 1953, uns prótesis cementada autobloqueante, como modificación de la Thomson.
En 1971, Galante demuenstra la utilidad de una superficie poriosa con mañlas de titanio en als prótesis de cadera.
En 1975, Mitterlmeier crea una prótesis de vástago recto y componente acetabular roscado con cabeza y cotilo de cerámica, para mejorar el componente de fricción.
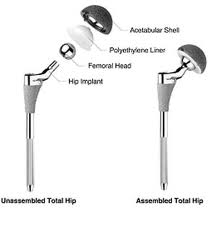
Los componentes básicos de una prótesis de cadera son:
Cabeza, la parte que sustituye a la cabeza femoral y la que va a articularse sobre el inserto y cotilo para dar la rotación de la movilidad de la cadera.
 |
| Cabeza |
Inserto, parte que encaja en el cotilo y sobre la que articula la cabeza, forma el par de fricción de la cadera.
 |
| Inserto |
Cotilo, parte que encaja en el acetábulo de la cadera, y sobre el que se acopla el inserto.
 |
| cotilo |
Vástago, parte distal de la prótesis, se introduce dentro del canal del fémur, como el resto de componentes tiene diferentes medidas para adaptarse a la anatomía del paciente, sobre su parte craneal se acopla la cabeza que como veremos puede ser de diferentes materiales, para completar la articulación sustituída.
 |
| Vástago |
Existen muchos tipos de prótesis de cadera, en función del tipo de lesión, fractura o patología tenga el paciente a intervenir, a cada año la medicina sigue avanzando y salen al mercado nuevas prótesis cada vez mas adaptadas y nuevos materiales, mas resistentes y duraderos.
Todas las prótesis de cadera se pueden cementar o no cementar en función de las características del hueso, la fractura o patología, la técnica empleada o la prótesis requerida.
Por tanto pueden ser Cementadas, no cementadas o híbridas ( un componente cementado y otro no cementado).
Sin embargo, en líneas generales podemos dividir las diferentes prótesis en 4 grandes grupos:
1.- Prótesis parciales:
Son las más conservadoras, sustituyen únicamente la parte mas proximal del fémur ( la cabeza femoral), no requieren el fresado del acetábulo por lo que a parte de conservar hueso en el fémur, también lo conservamos en el cotilo.
Entre estas podemos encontrar:
 |
| Thompson |
 |
| Moore |
Estas dos son en «bloque», la cabeza va unida directamente sobre el vástago.
 |
| Bipolar |
2.- Prótesis Total:
dependerá del material sobre el que friccione la cabeza femoral:
- Metal-polietileno
- Cerámica-polietileno
- Cerámica-cerámica
- Metal-metal
El motivo por el que se escoja cada par de fricción dependerá, de la movilidad de la cadera, la edad y actividad del paciente, el estado basal del paciente…
Os pego una explicación que viene muy detallada:
8.1. Par metal-polietileno
Sigue siendo el más utilizado. El polietileno, al friccionar con el metal libera partículas responsables de la llamada enfermedad por partículas. A cabezas mayores, más movilidad, mayor grado de fricción y más liberación de partículas, por lo que históricamente se tendía al uso de cabezas pequeñas. Los nuevos polietilenos de ultra alto peso molecular consiguen unos índices de fricción muy bajos y debido a su procesamiento (que aumentan los enlaces químicos internos altamente entrecruzados o cross-linked) disminuyen la liberación de partículas, mejorando la incidencia de la enfermedad por partículas que tenían los polietilenos previos, incluso utilizando cabezas más grandes y polietilenos más estrechos. El procesamiento del polietileno es también el menos costoso de los materiales articulares.
8.2. Par metal-metal
• Ventajas– Bajo desgaste y elevada supervivencia: preferible en pacientes jóvenes.– Autopulido: las superficies de las últimas generaciones del par metal-metal se autopulen con el movimiento, disminuyendo el desgaste, pero aumentando los niveles de partículas en sangre y orina.• Inconvenientes– Producción elevada de iones metálicos: se ha descrito la diseminación sistémica de los productos de la corrosión articular. Se pueden evidenciar niveles plasmáticos y en orina de iones, que podrían servir como marcadores de la evolución de la artroplastia. El portador de prótesis con este par de fricción presenta unos niveles de una a cinco veces mayor de iones en sangre que el paciente sano.– Producción elevada de partículas metálicas: se produce un mayor número de partículas que con el par metal-polietileno, pero son de mucho menor tamaño (< 50 nm). Estas partículas no producen una respuesta autoinmune como las partículas de polietileno, por lo que no se ha comprobado tanta osteolisis. Se desconoce la razón de este hecho y se atribuye a varias razones, como que los macrófagos capten las partículas por linfocitosis en lugar de por fagocitosis, o que una alta concentración de partículas produzca tal citotoxicidad que evite la respuesta celular, etc. 10,11 .– Riesgo de carcinogénesis y teratogénesis: no se conoce el efecto a largo plazo del par metal- metal. No se conocen las consecuencias de las altas concentraciones de iones metálicos en sangre y orina, pero se ha correlacionado la aparición de carcinomas en estudios con animales de experimentación con altos niveles de iones (Co, Cr, Ni). En humanos no se ha podido correlacionar. Se conoce que la aparición de cáncer (melanoma, próstata) tras artroplastia tiene una incidencia de 0,95 con par metal-metal, y del 0,76 en el par metal-polietileno no existiendo diferencias significativas 12,13 . Las pequeñas partículas metálicas también atravesarían la placenta pudiendo producir alteraciones teratogénicas, por lo que no se recomienda el par metal-metal en mujeres de edad fértil.– Hipersensibilidad: en pacientes susceptibles, los iones actúan como antígenos que activan el sistema inmune (linfocitos T). El níquel sería el metal que más produce esta hipersensibilidad, seguido del cobalto y del cromo. La prevalencia de hipersensibilidad en portadores de prótesis de cadera con par metal- metal se estima en 2/10.000.Debido a la alta duración del par M-M, existe una alta probabilidad de desarrollar una hipersensibilidad retardada. Si esto se produce y se necesita un recambio protésico se recomienda modificar el par de fricción.Según lo referido hasta aquí el par metal-metal está indicado para los pacientes más jóvenes, que no sean mujeres en edad fértil, con una función renal conservada. No se recomienda en ancianos ni en pacientes con antecedentes de hipersensibilidad a los metales.
8.3. Par cerámica-cerámica
Las cerámicas incluyen múltiples compuestos no metálicos que se fabrican mediante un proceso de horneado o cocción 14,15 . Se producen así estructuras en diferentes fases cristalinas (cristales amorfos, policristalinas o monocristalinas) con diferentes características biológicas. En general, presentan una alta biocompatibilidad y resistencia a la compresión, pero son muy frágiles. Poseen una escasa deformación plástica y ante la presencia de pequeñas muescas o grietas en la superficie, se concentran allí las tensiones de carga y la cerámica se fractura directamente, sin producirse deformación. Su módulo de elasticidad es muy diferente al hueso, por lo que no transmite las cargas de forma uniforme, incluso siendo altamente exigentes en la colocación de los componentes protésicos. En prótesis total de cadera esta característica favorece los aflojamientos del componente acetabular y la osteolisis local, por lo que no se aconseja que ambos componentes sean de cerámica.Su superficie es hidrofílica por lo que el líquido sinovial penetra muy bien en la superficie articular y disminuye mucho el coeficiente de fricción.Las más utilizadas son la alúmina (óxido de aluminio, Al 2 O 3 ), la circona (óxido de zirconio, ZrO 2 ) y la mezcla de ambas.• Alúmina: sustancia estable e inerte, no desprende subproductos ni sufre corrosión como los metales. Altamente biocompatible, no produce efectos inflamatorios, ni citotóxicos, ni carcinogenéticos. Mecánicamente es muy rígida. Su escasa deformación favorece la consecución de superficies muy precisas y dada su dureza (mayor que la del cromocobalto) ésta superficie se desgasta mucho menos (gran resistencia al rayado). En contraposición, su escasa elasticidad y la diferencia del módulo de elasticidad respecto al hueso, favorecen su rotura. En artroplastia de cadera se utilizan preferiblemente cabezas de alúmina de mayor tamaño (28 mm y 36 mm) (tabla 1).• Circona: mantiene las características de biocompatibilidad de la alúmina, pero incrementa sus propiedades mecánicas (mejora del desgaste lineal, volumétrico y de la resistencia) lo que permite trabajar, en artroplastia de cadera, con tamaños menores (cabezas de 22 mm y 28 mm). El comportamiento de la circona con polietilenos de ultra alto peso molecular es similar al de alúmina-UHMWPE.En contraposición, la estructura microcristalina de la circona presenta dudas acerca de su estabilidad porque se han recogido casos de desgastes catastróficos en periodos cortos de tiempo. En medio acuoso se ha compro bado que se puede producir el desgaste de la superficie de la circona, observándose un decremento en las propiedades mecánicas de la circona y un aumento del desgaste del otro par articular (polietileno o circona). Para intentar evitar estas alteraciones de la estructura microcristalina de la circona in vivo se fabrican nuevas cerámicas que incorporan itria (óxido de itrio, Y 2 O 3 ). Serán necesarios más estudios a largo plazo para analizar su durabilidad.Los pares que incluyan cerámica (cerámica-polietileno) son apropiados en pacientes jóvenes y también en mujeres en edad fértil, así como en pacientes con alteraciones renales puesto que no liberan iones metálicos. Los pares cerámicacerámica son menos utilizados al no poseer un módulo de elasticidad similar al hueso y ello favorece la presencia de aflojamientos protésicos.
8.4. Enfermedad por partículas
Los tejidos que rodean a una prótesis (sinovial, macrófagos, células gigantes de cuerpo extraño) fagocitan el acúmulo de partículas existentes en la articulación. Como consecuencia de ello la sinovial se engruesa y las células liberan mediadores inflamatorios (citoquinas, interleuquina y prostaglandinas) que tienen un efecto osteolítico y sobre la maduración de los osteoclastos. Esto aumenta la osteolisis periprotésica e inhibe la osteogénesis local, lo que favorece el aflojamiento precoz de los implantes. Los implantes cerámicos apenas liberan partículas y los implantes metálicos liberan muchas partículas de pequeño tamaño, que por causas no bien conocidas, escapan a la acción de los macrófagos locales. Por tanto, las principales partículas causantes de la enfermedad son las provenientes del polietileno.
Desgaste o rotura de alguno de los componentes por fricción de la articulación
Aflojamiento séptico o aflojamiento aséptico del implante.
Buscan el reemplazo de la zona afectada y habitualmente de forma mas distal que la prótesis primaria.
La dificultad para retirar la prótesis inicial, condiciona el transcurso de la cirugía, si será cementada o no, el uso de injerto óseo, etc.
 |
| Revisión |
4.-Prótesis tumorales:
Son aquellas que se utilizan para reconstruir la parte ósea que se pierde a causa del tumor, bien por la resección del mismo, bien la propia destrucción ósea que produce, pueden sustituir incluso la parte de la diáfisis femoral.



Estoy comenzando mi andanza por la trauma y la verdad esque este artículo me ha resultado de gren utilidad. Es una buena idea publicar este tipo de artículos que nos sirven de repaso y nos ayudan a entender mejor lo que hacemos, gracias
Me gustaMe gusta
Yo tambien les doy las gracias por este tipo de publicaciones ya que son de gran utilidad lara las personas que hemos sido intervenidas quirurgicamente yo cuento con 34 años y tengo una protesis thompson calibre 42 mm el doctor prometio volver a intervenirme para realizarme protesis total si tienen algun comentario al respecto dejo mi correo iconosolo@gmail.com GRACIAS!!!!!
Me gustaMe gusta